Patientenfall von Dr. Nikolina Witwer, LKH Hohenems, Innere Medizin

Foto Credit: Carmen Mayer
Anamnese
Im Dezember 2022 wurde eine bis dato gesunde 54-jährigen Patientin zur Abklärung einer Hämatochezie an
unsere Abteilung zugwiesen.
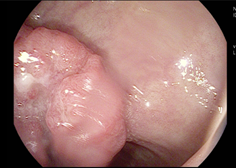
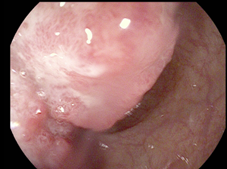
Als Ursache für die Blutung zeigten sich zwei Rektumkarzinome, eines im mittleren Rektumdrittel, das
zweite am rektosigmoidalen Übergang.
Zum Zeitpunkt der Diagnosestellung wurde ebenfalls eine disseminierte, nicht resektable Lebermetastasierung
festgestellt.
Somit wurden (nach molekularpathologischer Aufarbeitung) folgende Stadien für die beiden Tumore festgelegt:
Synchrone Adenokarzinome des Rektums bzw. rektosigmoidalen Überganges:
- Rektum: 5cm ab ano, cT3 cN2 cM1 (hep) UICC IVa,
- Rektosigmoidal: cT3 cN2 cM1 (hep) UICC IVa,
- Molekulares Profil (der Primaria im Darm): MSS, Her2neg, KRAS/NRAS/BRAF: WT
Prozedere:
Nach Beginn einer systemischen Chemotherapie nach dem modifiziertem FOLFOX6 Schema in Kombination mit
Panitumumab wurde im interdisziplinären Tumorboard der Wechsel auf eine Chemotherapie-Triplette +
anti-EGFR-Antikörper mit dem Ziel einer bestmöglichen Metastasenverkleinerung und Erreichen einer technischen
Operabilität beschlossen. Die Entscheidung basierte zu diesem Zeitpunkt auf den Daten der Phase II VOLFI-Studie.
Sie zeigte unter Chemotherapie-Triplette + Panitumumab hohe Remissionsraten und konsekutiv verbesserte
Resektionsraten. Eine Verbesserung des Gesamtüberlebens wurde jedoch nicht gezeigt.1
Verlauf:
Im März 2023 konnte nach zwei Zyklen (= vier Gaben) FOLFOXIRI + Panitumumab erfreulicherweise eine partielle
Remission erzielt werden. Wiederum erfolgte die Diskussion des Falles und Sichtung der aktuellen Bildgebung im
interdisziplinären Tumorboard, wo eine partielle Hemihepatektomie rechts und RFA links, gefolgt von einer
weiteren Systemtherapie für zwei Monate beschlossen wurde.
Intraoperativ musste der geplante Eingriff jedoch aufgrund des makroskopischen Verdachtes auf eine „blue liver“
abgebrochen werden. Lediglich die Gallenblase, eine Lebermetastase und ein Lymphknoten im Leberhilus wurden
entfernt.
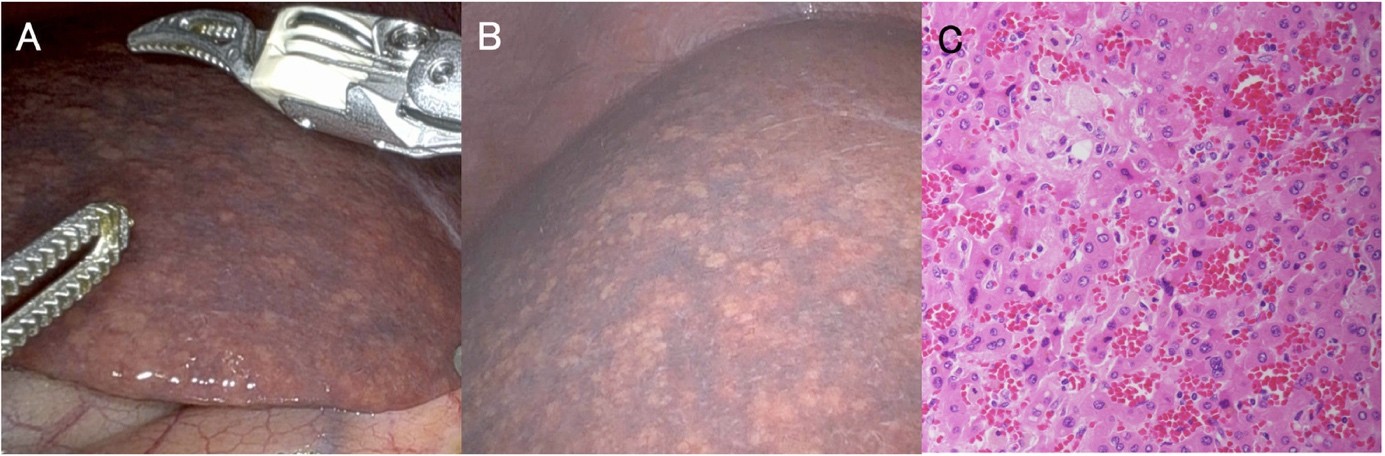
Exkurs: blue liver
Beim „Blue liver Syndrom“ (Oxaliplatin-induziertes sinusoidales Obstruktionssyndrom) liegt eine
Chemotherapie-assoziierte, sinusoidale Obstruktion (SOS) der Leber vor, die zu einem Ödem und in weiterer Folge
auch zu zentrolobulären Nekrosen und Atrophie führen kann. Die spongiforme Leberkonsistenz führt zu einer
makroskopisch bläulichen Verfärbung der Leber.2,3
Bei anhaltender Schädigung durch Oxaliplatin kann es in schweren Fällen zu einer nodulär-regenerativen
Hyperplasie kommen, welche letztendlich eine portale Hypertension ohne Zirrhose oder erhöhte
Leberfunktionsparameter zur Folge hat.2,3
Risikofaktoren für die Entwicklung eines Blue liver Syndroms sind die kumulative Platindosis, vorbestehende
Lebererkrankungen, allen voran die MASLD (Metabolic Dysfunction-Associated Steatotic Liver Disease) und eine bei
Behandlungsbeginn bestehende Splenomegalie.
Für eine frühzeitige Detektion eines Chemotherapie-induzierten Leberschadens eignet sich klinisch vor allem das
Monitoring der Milz mit frühzeitigem Erkennen einer neuauftretenden/aggravierten Splenomegalie, sowie die
Thrombopenie (welche allerdings auch differentialdiagnostisch auf die CTX-induzierte Knochenmarkstoxizität
zurückgeführt werden kann).
Weiterer Verlauf:
Bei unserer Patientin ließ sich histologisch in der zusätzlich durchgeführten Leberbiopsie kein
Leberschaden nachweisen. Die Systemtherapie wurde zwischenzeitlich mit FOLFIRI + Panitumumab (80%)
durchgeführt.
Nach drei Zyklen (=6 Gaben) zeigte sich bildgebend eine partielle Remission. Somit wurde im August 2023 eine
simultane Resektion der Rektumkarzinome sowie eine links laterale Wedge-Resektion der Leber durchgeführt. Zwei
Monate später erfolgte ergänzend noch die stereotaktische Radiofrequenzablation einer Metastase im rechten
Leberlappen.
Bildgebend zeigte sich im November 2023 ein neuaufgetretener Lungenrundherd, der stereotaktisch bestrahlt und
additiv mit FOLFIRI behandelt wurde.
Im Mai 2024 kam es zu einem Progress mit sechs neuen Lebermetastasen, einer peritonealen Absiedelung im kleinen
Becken und pulmonalen Metastasen.
Somit musste der kurative Therapieansatz definitiv auf ein palliatives Vorgehen umgestellt werden. FOLFIRI +
Panitumumab wurde re-Induziert, worunter sich zunächst wiederum ein gutes Ansprechen zeigte. Nach 8 Monaten kam
es zu einem neuerlichen Fortschreiten der Erkrankung, woraufhin die Therapie auf ein modifiziertes FOLFOX6
Schema + Bevacizumab umgestellt wurde.
Seit nunmehr 12 Monaten zeigt sich die Patientin unter dieser Therapie, welche aufgrund einer Polyneuropathie
CTCAE II-III° dosisreduziert werden musste, stabil. Zudem erfolgten auf Wunsch der Patientin mehrfache, 1-2
Monate dauernde Therapiepausen im Sinne von Drug-holidays.