Beim EHA 2025 wurden zu Blinatumomab Daten über das gesamte Zulassungsspektrum, von der Erstlinie über das MRD+-Setting bis hin zum Rezidiv, vorgestellt sowie eine weitere Analyse der Subkutanstudie. Diese wurde parallel in
Lancet Hematology veröffentlicht.
R/R BCP-ALL
“Safety and Efficacy of Single-Agent Subcutaneous Blinatumomab in Adults with Relapsed/Refractory (R/R) B-Cell Acute Lymphoblastic Leukemia (B-ALL). Results From a Phase 1/2 Dose Expansion Study” – Jabbour et al. S112
Nachdem beim
ASH 2024 bereits interessante Daten zur subkutanen
Blinatumomab-Formulierung vorgestellt wurden, folgten beim EHA 2025 die Ergebnisse der Dose-Expansion-Kohorten in den hohen Dosierungen (250 µg/ 500 µg bzw. 500 µg/ 1000 µg).
Ergebnisse
Wirksamkeit
Nach der initialen Dosisfindung wurden in die zwei Dose-Expansion-Kohorten insgesamt 36 (250 µg/ 500 µg) bzw. 52 (500 µg/ 1000 µg), teils stark vorbehandelte Patient:innen eingeschlossen. Abbildung 1 zeigt eine Zusammenfassung der
wichtigsten Patientencharakteristiken.

Abbildung 1 Patientencharakteristiken der Dose-Expansion-Kohorten
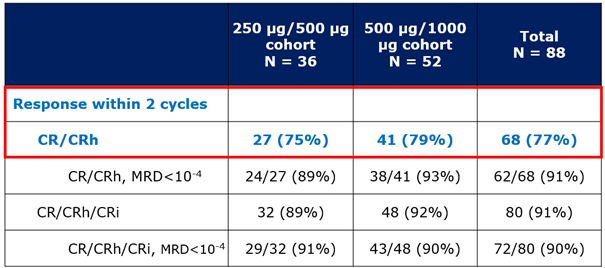
Der primäre Endpunkt, die Ansprechsrate (CR/CRh) innerhalb der ersten 2 Zyklen, lag in der 250 µg/ 500 µg-Kohorte bei 75 % (27/36), wovon 89 % eine MRD-Negativität (10-4) erreichten. In der Kohorte 500 µg/ 1000 µg waren es 79 %
(41/52) bzw. 93 % (38/41) (s. Tabelle 1).
Tabelle 1 Ansprechsraten nach 2 Zyklen Blinatumomab
Hierbei konnte auch bei den Patient:innen, die mit Blinatumomab (n=17), einer CAR-T-Zell-Therapie (n=14) oder Inotuzumab Ozogamicin (n=29) vorbehandelt waren, oder bereits eine HSZT erhalten hatten (n=25), ein Ansprechen beobachtet
werden (CR/CRh: 65 – 69%). Patient:innen mit einer BM-Blastenlast von <50 % bei Einschluss (n=33) hatten eine etwas höhere Ansprechrate (85 %) im Vergleich zu Patient:innen mit einer hohen Blastenlast (n=54; 72 %).
Nach einem medianen Follow-Up von ca. 6 bzw 7 Monaten lag das geschätzte 12-Monats-OS in den beiden Kohorten bei 63 % bzw. 70 %.
Verträglichkeit
Tabelle 2 fasst die wesentlichen behandlungsbedingten unerwünschten Ereignisse zusammen.
Tabelle 2 Behandlungsbedingte unerwünschte Ereignisse
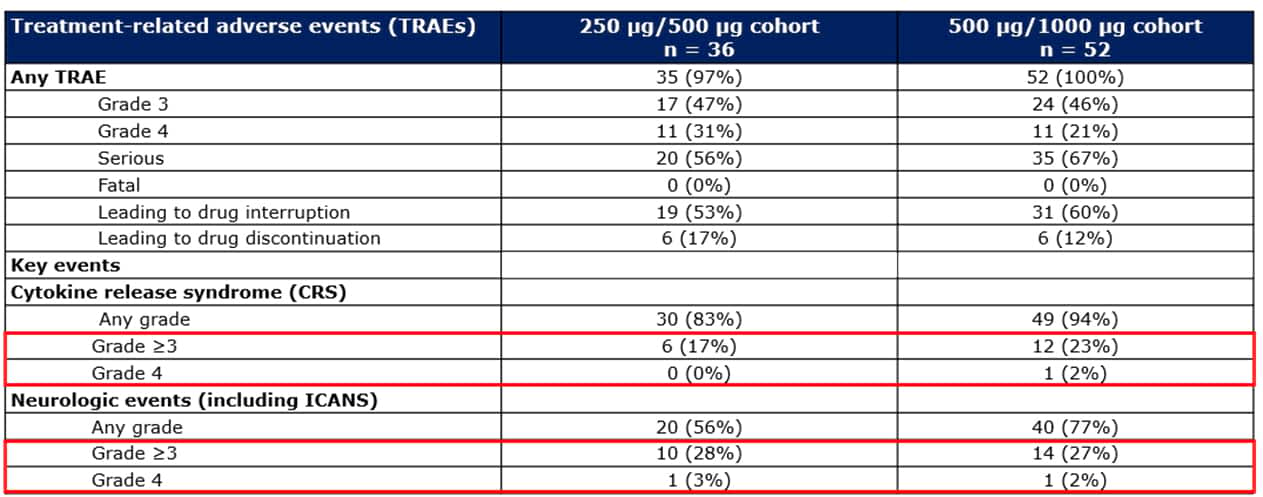
Die meisten CRS- und neurologischen Ereignisse verschwanden mit einer Unterbrechung der subkutanen Blinatumomab-Behandlung und/oder unterstützenden Pflegemaßnahmen wie Kortikosteroiden, i.v. Flüssigkeiten, Antipyretika und/oder
Tocilizumab, ohne Absetzen von Blinatumomab.
Fazit:
Blinatumomab in der subkutanen Formulierung zeigte in beiden Dosis-Kohorten hohe Ansprechs- und MRD-Negativitätsraten. Die Dosierung 250 µg/ 500 µg wurde als RP2D festgelegt.
Die Slides können Sie
hier herunterladen.




