Beim KRAS G12C mutierten mCRC gab es interessante Daten bei chemorefraktären Patient:innen:
“Combined Analysis of Overall Survival (OS) From the phase 3 CodeBreaK 300 and
Phase 1b CodeBreaK 101 Studies of Sotorasib 960 mg Plus Panitumumab (soto960+pani) Therapy for Chemorefractory
KRAS G12C-Mutated Metastatic Colorectal Cancer (mCRC)” – Kuboki et al. 743P
Die Kombination aus Sotorasib (960mg) + Panitumumab zeigte in den Phase 1b CodeBreaK 101 und Phase 3 CodeBreaK 300
Studien vielversprechende Wirksamkeit gegen chemorefraktäre KRAS G12C-mutierte metastasierte Kolorektalkarzinome
(mCRC).
Diese post-hoc Studie kombinierte Daten zu Gesamtüberleben aus beiden Studien (n=93, CodeBreak 300 n=53, CodeBreak
101 n=40), um die Langzeitwirksamkeit (2-Jahre) von Sotorasib + Panitumumab zu bewerten.
Ergebnisse:
Wirksamkeit:
Mit 13,2 Monaten zeigten Patient:innen ein längeres Gesamtüberleben im Vergleich zu Standardbehandlungen (6,4 – 10,8
Monate) (Abbildung 1).
Die 2-Jahres-Gesamtüberlebensrate von 23%, bei einem mittleren Follow-Up von 28,1 Monaten ist vielversprechend für
Patient:innen mit KRAS G12C-mutiertem mCRC.
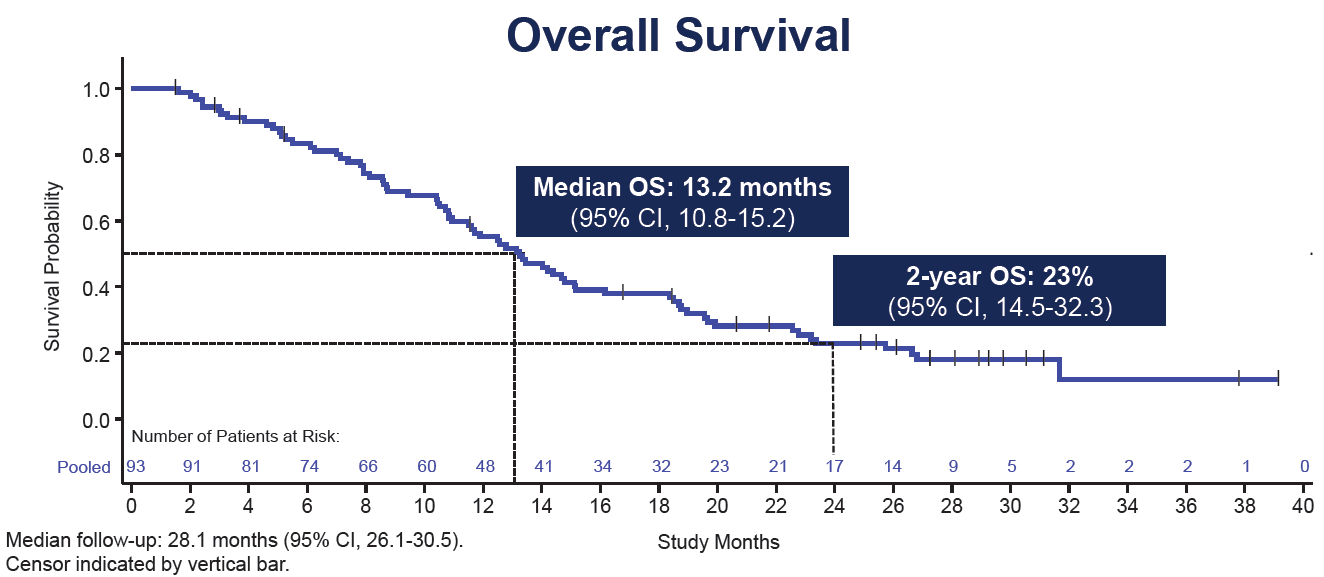
Abbildung 1: Gesamtüberleben für Patient:innen mit
Sotorasib + Panitumumab in Monaten.
Das mediane Gesamtüberleben in Monaten war in den analysierten Subgruppen weitgehend konsistent, mit Unterschieden
hinsichtlich Alter (<65: 12,5 vs. ≥65: 16,6), Region (Asien: 16,2, Europa: 11,7, Nordamerika: 12,8) und Anzahl
der Metastasierungsorte (1: 14,5, 2: 12,6, 3: 14,7, >3: 6,2).
49 von 93 (53%) Patient:innen erhielten nach Abschluss der Studienbehandlung eine Krebstherapie, meist
Fluoropyrimidin (42%), Regorafenib oder Trifluridin (34 %), oder Bevacizumab (28%).
Verträglichkeit:
Die Analyse der langfristigen Verträglichkeit von Sotorasib + Panitumumab ergab keine neuen Erkentnisse zu
unerwarteten Nebenwirkungen.
Das Poster können Sie
hier herunterladen.
“FOLFOX plus PANITUMUMAB (Pmab) according to a “stop-and-go” strategy in
first-line in patients (pts) with non-mutated RAS/BRAF metastatic colorectal cancer (mCRC). Results of the FFCD
1605 – OPTIPRIME phase II trial” – Bachet et al.
Eine Kombination aus Chemotherapie-Dublette (FOLFOX) mit einem
Anti-EGFR-Antikörper ist eine Standard-Erstlinientherapie bei RAS/BRAF-Wildtyp mCRC.
In dieser nicht randomisierten Phase 2 Studie wurde eine „Stop and Go“ Behandlungsstrategie von Panitumumab +
Chemotherapie untersucht, um die kumulative Toxizität und Resistenzentwicklung zu verringern.
Ergebnisse:
115 Patient:innen, ohne vorherige systemische Therapie, mit ECOG 0–2 und inoperablen Metastasen, erhielten mFOLFOX6
+ Panitumumab für 6 Zyklen als Induktion, gefolgt von LV5FU2 oder Capecitabin als Erhaltung bei
komplettem/partiellem Ansprechen oder stabiler Krankheit. Bei Progression wurde mFOLFOX6 + Panitumumab reinduziert.
Diese Behandlungszyklen waren mehrfach möglich und wurden bis zur Progression oder Toxizität durchgeführt.
Wirksamkeit:
Bei einem medianen Follow-Up von 47,9 Monaten, erhielten 100% der Patient:innen die Induktionstherapie und 83,5% die
erste Erhaltungstherapie. Die erste Reinduktion wurde bei 54% durchgeführt, 25% erhielten eine zweite Reinduktion,
und 10% eine dritte Behandlung mit mFOLFOX6 + Panitumumab.
Die Dauer der Krankheitskontrolle betrug 24,9 Monate (Abbildung 1). Nach 82 Ereignissen (71,3%) betrug das
Gesamtüberleben 36,1 Monate.
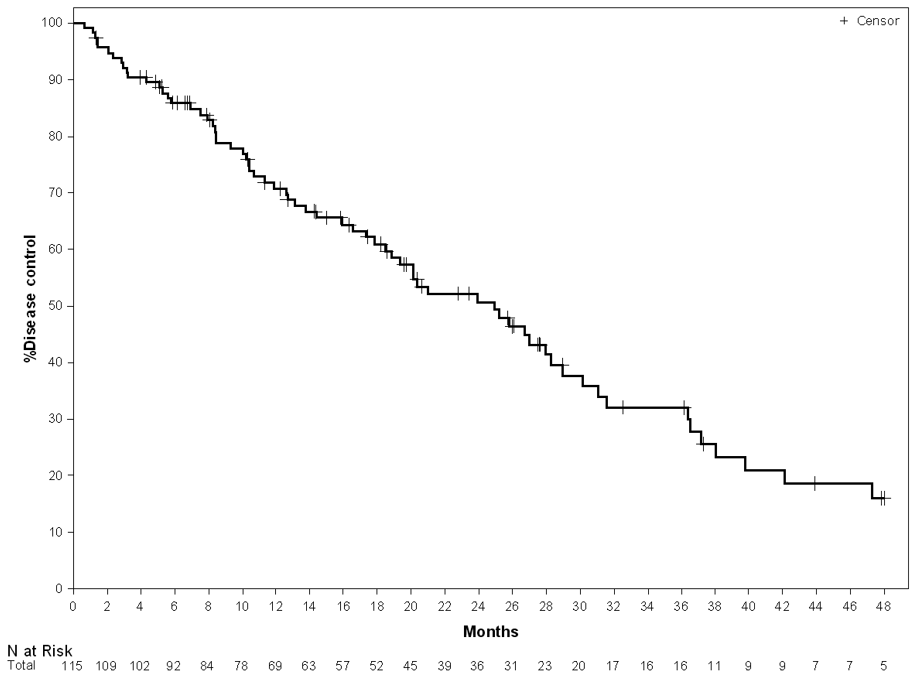
Abbildung 2: Dauer der Krankheitskontrolle in
Monaten.
Die objektive Ansprechrate und das progressionsfreie Überleben verringerten sich mit jedem Behandlungszyklus
(Tabelle 1).
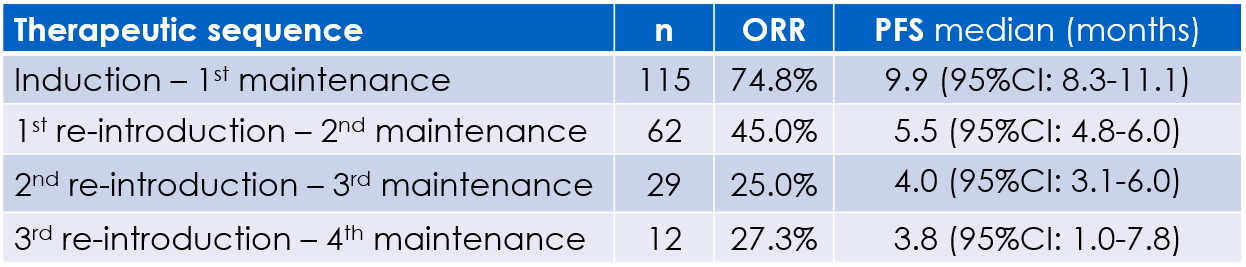
Tabelle 1: Wirksamkeit der Behandlung nach den
Therapie-Zyklen.
Gründe für die Beendigung der Behandlung waren Progression (50%), Toxizität (16%), Resektion der Metastasen (11%),
klinische Entscheidung (8%), und Tod (6%). 69,6% der Patient:innen erhielten eine zweite, und 53% eine dritte
nachfolgende Behandlung mit Chemotherapie.
Verträglichkeit:
Die Analysen zu Verträglichkeit und Lebensqualität sind noch nicht abgeschlossen.
Fazit:
Die Dauer der Krankheitskontrolle betrug 24,9 Monate bei „Stop and Go“ Behandlung mit Panitumumab + Chemo in der
Erstlinie, und das Gesamtüberleben entspricht aktuellen Phase 3 Studien. Die Wirksamkeit der Behandlung nimmt mit
jeder Reinduktion der Therapie ab. Diese Ergebnisse sind vergleichbar zu einer Erhaltungstherapie mit
Fluoropyrimidinen mit oder ohne Panitumumab aus der PANAMA-Studie. Diese Daten unterstützen eine Erhaltungstherapie
mit Fluoropyrimidinen allein.
Slides können Sie
hier herunterladen.
“Panitumumab retreatment followed by regorafenib versus the reverse sequence in
chemorefractory metastatic colorectal cancer patients with RAS and BRAF wild-type circulating tumor DNA (ctDNA):
Final results of the randomized PARERE trial by GONO” – Germani et al.
Bei vorbehandelten Patien:innen mit RAS/BRAF-Wildtyp mCRC ist eine erneute Behandlung mit Anti-EGFR Therapien
vielversprechend. In der REVERCE-Studie zeigte Regorafenib → Cetuximab ein längeres Gesamtüberleben als Cetuximab →
Regorafenib.
In dieser randomisierten Phase 2 Studie wurde analysiert, ob Panitumumab → Regorafenib oder die umgekehrte
Reihenfolge der Behandlung einen Effekt auf das Gesamtüberleben von Patient:innen mit mCRC hat.
Ergebnisse:
Patient:innen ≥ 18 Jahre mit ECOG ≤ 1, die bereits mit Fluoropyrimidinen, Oxaliplatin, Irinotecan, und
Angiogenesehemmern oder vor ≥ 4 Monaten mit 1L Anti-EGFR-Therapie behandelt wurden, bekamen entweder Panitumumab →
Regorafenib (n=106) oder Regorafenib → Panitumumab (n=107) bis zur Progression. Die Baseline-Charakteristika waren
zwischen den Behandlungsarmen in Bezug auf Alter, Geschlecht, und Ansprechen auf 1L Anti-EGFR, vergleichbar.
Wirksamkeit:
Bei einem Follow-Up von 31,9 Monaten wurde kein signifikanter Unterschied im Gesamtüberleben zwischen den
Behandlungsarmen gefunden (HR 1,13; 0,90–1,41; p = 0,44) (Abbildung 1).
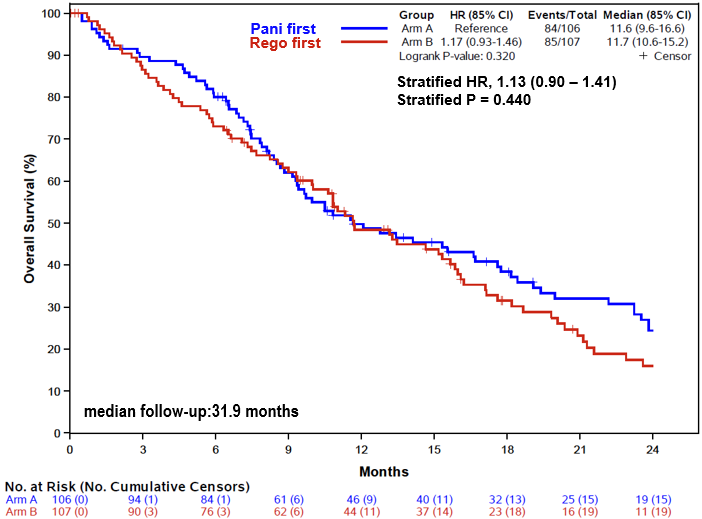
Abbildung 3: Gesamtüberleben in Monaten zwischen den Behandlungsarmen.
Nach einer molekularen Selektion von Patient:innen basierend auf Mutationen, die die Resistenz gegen EGFR-Therapien
nicht beeinflussen (AKT1, EGFR-ECD, ERBB2, MAP2K1, PIK3CA exon 20, BRAF class I/II non-V600E), konnten keine
Unterschiede im Gesamtüberleben zwischen den Behandlungsarmen festgestellt werden.
Eine wiederholte Anti-EGFR Therapie mit Panitumumab war in Bezug auf progressionsfreies Überleben, objektive
Ansprechrate, und Dauer der Krankheitskontrolle unabhängig von der Reihenfolge der Behandlung vorteilhaft.
Die Subgruppenanalyse ergab, dass weibliches Geschlecht und ein Intervall von > 6 Monaten ohne vorherige Anti-EGFR
Therapie mit einen längeren Gesamtüberleben bei Panitumumab → Regorafenib assoziiert waren. Patient:innen mit einem
Anti-EGFR-freien Intervall von ≤ 6 Monaten profitierten weniger von einer wiederholten Panitumumab Behandlung. Eine
vergleichbare Anzahl an Patient:innen erhielten Behandlungen nach Studienabschluss.
Verträglichkeit:
Die unerwünschten Nebenwirkungen traten mit der erwarteten Häufigkeit und zu vergleichbaren Raten zwischen den
Behandlungsarmen auf, wobei Akneiformer Ausschlag, Hypomagnesiämie, Fatigue, Hand-Fuß-Syndrom, und Hypertonie
typische Symptome waren.
Fazit:
Die Reihenfolge der Behandlung hat keinen Einfluss auf das Gesamtüberleben. Jedoch sollten wiederholte Behandlungen
mit Anti-EGFR Therapien frühzeitig angewendet werden und stellen eine vielversprechende Option nach Progression der
Krankheit oder bei Kontraindikationen als Drittlinientherapie bei mCRC dar.
Slides können Sie
hier herunterladen.





